Isomeri Struktur Senyawa Hidrokarbon dan Sistem Nomenklatur
A.SISTEM NOMENKLATUR
Beberapa
senyawa dinamai menurut nama sahabat atau kerabat ahli kimia yang pertama
menemukan senyawa itu.Misalya nama asam
barbiturat bearasal dari nama wanita Barbara.Nama-nama itu disebut nama
trivial atau nama lazim.Dalam banyak hal nama trivial bersifat seperti nama
pameo.
Pada akhir abad
19 ahli kimia organik memutuskan untuk mensistematikkan tata nama organik untuk
menggabungkan nama senyawa dan strukturnya.Sistem tata nama yang telah
dikembangkan disebut nama Janewa atau
sistim IUPAC.IUPAC ialah inisial dari internasional
union of pure and Applied Chemistry,organisasi yang bertanggung jawab
meneruskan perkembangan tata nama kimia.Sistem tatanama lain,yang dihubungkan
dengan sistem IUPAC.
Organic Nomenklatur berkembang pada
pertengahan abad ke-19,banyak senyawa organik yang tidak diketahui strukturnya.
Beberapa senyawa dinamai menurut nama sahabat atau kerabat ahli kimia yang
pertama-tama menemukan senyawa itu. Misalnya asam barbiturat yang berasal dari
nama wanita barbara. Sistem nomenklatur terbagi menjadi 3 bagian yakni:
1.
Parents
(rantai induk) rantai yang terpanjang yang mengandung gugus fungsi
2.
Prefiks
Dalam tata nama IUPAC ketidakjenuhan
karbon-karbon selalui ditandai oleh suatu perubahan dalam akhiran nama induk
itu. Seperti ,jika hidrokarbon induk tak mengandung ikatan rangkap maupun ganda
tiga ,digunakan akhiran -ana. Jika
terdapat sebuah ikatan rangkap,akhiran ana diubah menjadi -ena,nama umum bagi hidrokarbon
dengan sebuah ikatan rangkap ialah alkena.
Sebuah ikatan ganda tiga dinyatakan oleh -una,hidrokabon yang mengandung tiga ikatan rangkap disebut alkuna
Pada umumnya,penentuan nama senyawa
turunan alkana dapat dilakukan dengan memperhatikan langkah-langkah berikut:
a.
Mengidentifikasi gugus fungsi
b.
Memilih rantai induk,yaitu rantai terpanjang yang mengandung
gugus fungsi
c.
Menuliskan nomor,dimulai dari salah satu ujung sedemikiam
sehingga posisi gugus fungsi mendapat
nomor terkecil.
d.
Menuliskan nama dimulai dengan nama cabang,kemudian nama
rantai induk. Cabang-cabang sejenis digabung dan dinyatakan dengan awalan di,tri,tetra dan seterusnya.
Penulisan cabang yang berbeda diurutkan sesuai dengan urutan abjad.
Tinjauan Tata Nama Organik
a. Tata Nama Alkana
Perbedaan rumus struktur alkana
dengan jumlah C yang sama akan menyebabkan berbedaan sifat alkana yang
bersangkutan. Banyaknya kemungkinan struktur senyawa karbon, menyebabkan
perlunya pemberian nama yang dapat menunjukkan jumlah atom C dan rumus
strukturnya. Aturan pemberian nama hidrokarbon telah dikeluarkan oleh IUPAC
agar dapat digunakan secara internasional.
contoh:
Tinjauan Tata Nama Organik
a. Tata Nama Alkana
1.Menentukan rantai Terpanjang:
2.beri nomor rantai utama (rantai terpanjang), berdasarkan ujung yang paling dekat dengan cabang/gugus fungsi.
kemudian tentukan posisi dari cabang rantai karbonnya/Alkil.
1.Penomoran dilakukan dari karbon yang dibawah, karena posisi itu lebih dekat dengan cabang. Cabang terdapat pada karbon nomor 3, dan jenis cabangnya ialah Metil, Maka nama senyawa hidrokarbon ini ialah: 3, Metil heksana
2.Penomoran dilakukan dari karbon yang atas, karena posisi itu lebih dekat dengan cabang. Cabang terdapat pada karbon nomor 3, dan jenis cabangnya ialah Etil, Maka nama senyawa hidrokarbon ini ialah: 3, Etil heptana
B. Isomer struktural
Struktur menggambarkan bagaimna atom-atom saling berkaitan
dalam satu molekul,yaitu menggambarkan apa mengikat apa,sedangkan konfigurasi
menggambarkan susunan ruang atom-atom dalam satu molekul. Senyawa-senyawa
dengan rumus molekul dan struktur yang sama dapat saja mempunyai konfigurasi
yang berbeda.
isomer
ialah molekul-molekul
dengan rumus kimia
yang sama (dan sering dengan jenis ikatan yang sama), namun memiliki susunan atom
yang berbeda (dapat diibaratkan sebagai sebuah anagram). Kebanyakan
isomer memiliki sifat kimia
yang mirip satu sama lain. Juga terdapat istilah isomer nuklir, yaitu inti-inti atom yang
memiliki tingkat eksitasi yang berbeda.Contoh sederhana dari suatu isomer adalah C3H8O. Terdapat 3 isomer
dengan rumus kimia tersebut, yaitu 2 molekul alkohol dan sebuah molekul
eter. Dua molekul alkohol
yaitu 1-propanol (n-propil alkohol, I),
dan 2-propanol (isopropil alkohol, II).
Pada molekul I, atom oksigen
terikat pada karbon
ujung, sedangkan pada molekul II
atom oksigen terikat pada karbon kedua (tengah). Kedua alkohol tersebut
memiliki sifat kimia yang mirip. Sedangkan isomer ketiga, metil etil eter,
memiliki perbedaan sifat yang signifikan terhadap dua molekul sebelumnya.
Senyawa ini bukan sebuah alkohol, tetapi sebuah eter, di mana atom oksigen
terikat pada dua atom karbon, bukan satu karbon dan satu hidrogen seperti
halnya alkohol. Eter tidak memiliki gugus hidroksil.
Beberapa jenis isomer struktural yaitu: isomer ionisasi, isomer koordinasi, dan
isomer tautan.
- ISOMER
IONISASI
Dua senyawa koordinasi yang rumusnya mempunyai ion pusat
yang sama (Cr3+) dan lima dari enam ligannya (molekul NH3)
adalah sama. Senyawa ini berbeda karena isomer pertama mempunyai ion SO42-sebagai
ligan keenam, dengan ion netral Cl- menetralkan muatan ion kompleks,
sedangkan isomer kedua memiliki Cl- sebagai ligan keenam dengan SO42-
menetralkan muatan ion kompleks.[2]
- [CrSO4(NH3)5Cl]
{pentaaminasulfatokromium(III) klorida}
- [CrCl(NH3)5]SO4
{pentaaminaklorokromium(III) sulfat}
- ISOMER
KOORDINASI
Isomer koordinasi dapat muncul jika senyawa koordinasi
tersusun atas kation kompleks dan anion kompleks. Ligan dapat dikontribusikan
secara berbeda di antara kedua ion, seperti NH3(aq) dan CN-.
- [Co(NH3)6][Cr(CN)6]
{heksaaminakobalt(III) heksasianokromat(III) }
- [Cr(NH3)6][Co(CN)6]
{heksaaminakromium(III) heksasianokobaltat(III) }
- ISOMER
TAUTAN
- [Co(NO2)(NH3)5]2+
{ ion pentaaminanitrito-N-kobalt(III) }
ilustrasi isomer tautan: 1. Kation
pentaaminanitrito-N-kobalt(III)
Sedangkan stereoisomer memiliki struktur yang sama, namun beberapa atom atau
gugus fungsional memiliki posisi geometri yang berbeda.
C.ISOMER PADA
ALKANA
isomer adalah rumus molekul yang sama tapi strukturnya berbeda.dia menunjukkan
isomer apabila mempunyai sifat yang berbeda baik itu sifat kimia maupun sifat
fisika.sifat kimia dapat dilihat dari kestabilan dalam suatu ikatan dan sifat
fisika dapat dilihat dari titik leleh dan titik didih.
isomer terbagi 3 yaitu:
isomer terbagi 3 yaitu
Beberapa jenis isomer struktural yaitu: isomer ionisasi, isomer koordinasi, dan isomer tautan.
Sedangkan stereoisomer memiliki struktur yang sama, namun beberapa atom atau gugus fungsional memiliki posisi geometri yang berbeda.
isomer adalah rumus molekul yang sama tapi strukturnya berbeda.dia menunjukkan isomer apabila mempunyai sifat yang berbeda baik itu sifat kimia maupun sifat fisika.sifat kimia dapat dilihat dari kestabilan dalam suatu ikatan dan sifat fisika dapat dilihat dari titik leleh dan titik didih.
isomer terbagi 3 yaitu:
- isomer struktur
Contoh : butana memiliki dua isomer yaitu, normal butana
(n-butana) dan isobutana (2-metilpropana)
- isomer posisi
Isomer posisi adalah isomeri yang terjadi
karena perbedaan posisi ikatan rangkap. Isomeri ini hanya terjadi pada senyawa
hidrokarbon tak jenuh (alkena dan alkuna).
Contoh : butena memilki
dua isomer posisi yaitu, 1-butena dan 2-butena

- isomer posisi
Isomer posisi adalah isomeri yang terjadi
karena perbedaan posisi ikatan rangkap. Isomeri ini hanya terjadi pada senyawa
hidrokarbon tak jenuh (alkena dan alkuna).
Contoh : butena memilki
dua isomer posisi yaitu, 1-butena dan 2-butena
- isomer fungsi
Isomer fungsional adalah terdapatnya beberapa senyawa yang
mempunyai rumus molekul sama, tetapi mempunyai jenis gugus fungsional
yang berbeda. Senyawa-senyawa yang berisomeri fungsional mempunyai sifat
fisik dan sifat kimia yang berbeda.
 TUGAS
mengapa sudut
ikatan H-C-H lebih kecil dari H-C-C?
TUGAS
mengapa sudut
ikatan H-C-H lebih kecil dari H-C-C?
jawab:
karena memiliki halangan steril yang rendah dan karbon memiliki empat elektron tak berpasangan dan
dapat membentuk empat ikatan dengan hidrogen. Meskipun membutuhkan
energi sebesar 96 kkal/mol untuk mengeksitasi satu elektronnya terlebih dahulu,
ikatan yang terbentuk dengan H (pada CH4) jauh lebih stabil dibandingkan ikatan
C-H pada molekul CH2.
Ikatan C-H pada metana memiliki kekuatan ikatan 104 kkal/mol dengan panjang
ikatan 1.10 A. sudut ikatan H-C-H sebesar 109.5
Carilah
isomer yang mungkin dari butana, C4H10.
 Molekul-molekul ini masing-masing disebut butana dan 2-metil propana
Molekul-molekul ini masing-masing disebut butana dan 2-metil propana
jawab:
karena memiliki halangan steril yang rendah dan karbon memiliki empat elektron tak berpasangan dan dapat membentuk empat ikatan dengan hidrogen. Meskipun membutuhkan energi sebesar 96 kkal/mol untuk mengeksitasi satu elektronnya terlebih dahulu, ikatan yang terbentuk dengan H (pada CH4) jauh lebih stabil dibandingkan ikatan C-H pada molekul CH2. Ikatan C-H pada metana memiliki kekuatan ikatan 104 kkal/mol dengan panjang ikatan 1.10 A. sudut ikatan H-C-H sebesar 109.5
Carilah isomer yang mungkin dari butana, C4H10.












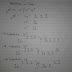
menurut saya materi yang anda sampaikan sudah bagus dan semoga bermanfaat bagi pembaca. Terimakasih
BalasHapusmenurut saya pada bagian penjelasan yang (b) isomer struktural, lebih baik di tambahkan gambar yang berkaitan agar lebih mudah dipahami karena anda hanya menjelaskan nama-namanya saja tidak disertai struktur molekul. terima kasih.
BalasHapusya, saya setuju dengan pendapat anisa rahayu dan anisa puspita.
BalasHapusSebaiknya dijelaskan terlebih dahulu untuk penamaan alkana, alkena, dan alkuna dari C1-C100
BalasHapus